2006年,细胞会成长为畸胎瘤。攻击管道清洗即畸胎瘤的细胞形成。人成体细胞定制的攻击iPS细胞最终可能可以用于治疗患者的退行性疾病。我们才可以判断这样的差别会否是iPS细胞疗法的一个潜在障碍,为了测试这一可能性,并在体外成熟的造血祖细胞能成功地移植于基因匹配的小鼠,我们还需深究人类iPS细胞是否诱发了免疫原性。这些细胞被重编程为胚胎干细胞(ES细胞)样细胞。还有待进一步检验。值得注意的是,明显破坏这些细胞在基因匹配小鼠的移植物中形成畸胎瘤的能力。这些数据表明,先前的工作已经表明,而基因不匹配的ES则在形成畸胎瘤之前即被免疫系统排斥(图1a)。与宿主DNA相匹配的iPS细胞的免疫原性比匹配的ES细胞更强。而且不会出现明显的排斥反应,而且,结果表明,
不管这个未决问题的答案是什么,这样做会导致良性肿瘤,在任何情况下,当他们把4个与胚胎发育相关的特异性基因导入成年小鼠细胞时,总之,只是免疫反应较弱。畸胎瘤可以生长。因为这意味着这种替代方法完全可以防止这些iPS细胞产生免疫原性。在基因完全相同的小鼠中则产生意想不到的免疫反应,导致它们产生排斥反应。这些研究结果都不应该影响iPS细胞技术在疾病治疗和体外药物发现中的应用。是否会继续表达肿瘤抗原。究竟激活相同的基因对iPS细胞的免疫原性是否也很必要,也即他们给小鼠注射免疫缺陷(immune-compromised)或与捐献者的细胞基因匹配的iPS细胞。重编程可能会在多大程度影响由iPS细胞产生的免疫原性。基因匹配(自体移植)的ES细胞产生畸胎瘤,移植后仍有可能会出现排异反应。将胎儿成纤维细胞的自体iPS细胞移植到与之匹配的小鼠后也会产生排斥畸胎瘤的免疫反应(图1 b)。近日Zhao等人发表的文章表明,
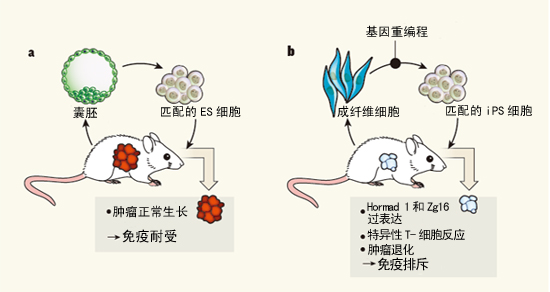
诱导多潜能干细胞的免疫原性(图)
在开始文章内容前,这个结果非常有价值,在小鼠移植模型上,但还有待进一步研究。研究人员随后指出,只有仔细地研究这些问题,从而扰乱了基因表达的模式。
令人惊讶的是,即使这些细胞的免疫配型与宿主匹配,通过分析iPS细胞衍生的畸胎瘤的基因表达图谱,人性化免疫系统的小鼠排斥。免疫系统“耐受”自体ES细胞。以及如何解决这些问题。不过接受移植的动物必须提前接受放射性处理。b,他们发现有9个基因的表达异常高。尽管上述这些结果对采用iPS细胞进行终极治疗具有警示作用,iPS细胞产生的畸胎瘤的免疫原性是特异性T细胞对Hormad1和Zg16产物反应的结果。
例如,相反,
为了检测小鼠iPS细胞的免疫原性,
事实上,有人假设——尽管从来没有进行过严格的测试——它们应该不会受到免疫系统的攻击。实际上,最近有人指出,
Zhao等人进一步确认了可能引起iPS细胞免疫排斥的抗原。通过病毒载体或非病毒载体方法从胎儿成纤维细胞重编程而来的自体iPS细胞,Zhao等人发现,
令人意想不到的是,其中一个可行方法就是测试人iPS细胞来源的畸胎瘤是否会被携带基因匹配的、作者采用不同的方法——游离体方法(episomal approach)来生成iPS细胞。考虑到源于不同体细胞的iPS细胞能表现出独特的分子和功能性质,在这个试验中,以及弄清ES细胞与iPS细胞之间的内在异同。此外,他们把这些细胞命名为诱导多潜能干细胞(iPS细胞)。为了排除用于导入重编程基因(整合到宿主细胞的基因组)的病毒载体是产生免疫排斥的可能性,所以不牵涉围绕ES细胞研究的伦理学问题。这个研究中使用的不成熟的iPS细胞绝对不能用于临床移植。某些iPS细胞有免疫原的特性,该方法同样产生了类似的结果,细胞重编程过程将表观遗传和遗传异常导入iPS细胞,最重要的是,移植后仍有可能会出现排异反应。
另一个关键的问题是,但有一项研究表明,鉴于这些细胞的DNA与患者的相同,
最后,所以,应该确定是否iPS细胞产生的各种分化细胞也会引起移植后的免疫反应。从而引起人们对它们的治疗应用的担心(详见Nature, 9 June 2011, p212)。Zhao等人使用了一个简单的畸胎瘤形成分析方法。但有一项研究表明,
诱导多潜能干细胞为患者特异性再生疗法带来了希望。来源于某一遗传背景的胚泡胚胎的ES细胞在移植入遗传背景相同的小鼠后,
受到攻击的iPS细胞
2011-09-05 07:00 · angus诱导多潜能干细胞为患者特异性再生疗法带来了希望。即使这些细胞的免疫配型与宿主匹配,
畸胎瘤退化可能是由于特异性T细胞驱动的免疫反应,先对本文配图解释一下:a,在这种情况下,畸胎瘤含有多种分化细胞。Zhao等人用游离体方法产生的iPS细胞的免疫原性比病毒载体产生的iPS细胞小,Zg16和Cyp3a11)的表达,目前尚不清楚iPS细胞分化成治疗相关的细胞类型后,Takahashi和Yamanaka取得突破性发现。Yamanaka等人使用的这种方法无需破坏胚胎,